一、膜蛋白:生命活動的“守門員”與藥物研發的“黃金靶點”
蛋白質是細胞生命過程的重要執行者,而膜蛋白所扮演的角色讓細胞得以成為生命的基本單元。從細菌到哺乳動物細胞,膜蛋白形成了眾多高度保守的蛋白質家族,是生物膜功能的主要承擔者,除了完成生物膜兩側的物質、能量和信息的傳輸,還擔負著生物膜的合成、穩態維持等任務,并且參與細胞之間及膜被細胞器之間的相互作用。正因為如此,膜蛋白與多種人類疾病密切相關,并且是直接的藥物靶標。
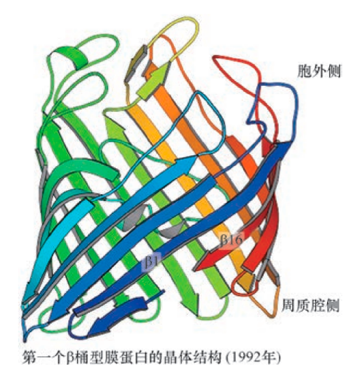
圖1: 典型β桶型膜蛋白E. coliOmp-F的晶體結構
然而,目前膜蛋白的研究仍然存在著較大差距:在人類基因組中,約30%的蛋白質基因參與編碼膜蛋白(其余編碼水溶性蛋白質);但膜蛋白僅占蛋白質數據庫(PDB)中沉積結構的約 3.6%(根據截至 2021 年 11 月的 PDBTM 數據庫)。由此也可以看出膜蛋白的結構和功能研究擁有著廣闊的發展空間。
二、結構決定功能:膜蛋白的核心類型
膜蛋白分為錨定蛋白和跨膜蛋白(又稱為整合型膜蛋白),后者作為膜蛋白的核心亞型,對于所有生物體維持各種生物學功能至關重要,是物質跨膜轉運、跨膜信號傳遞等關鍵過程的主要執行者。例如,離子通道、葡萄糖轉運蛋白、G蛋白偶聯受體等均為跨膜蛋白,其功能直接決定了細胞與外界環境的物質交換效率和信號響應能力,也是后續深入研究膜蛋白功能與應用的核心對象。
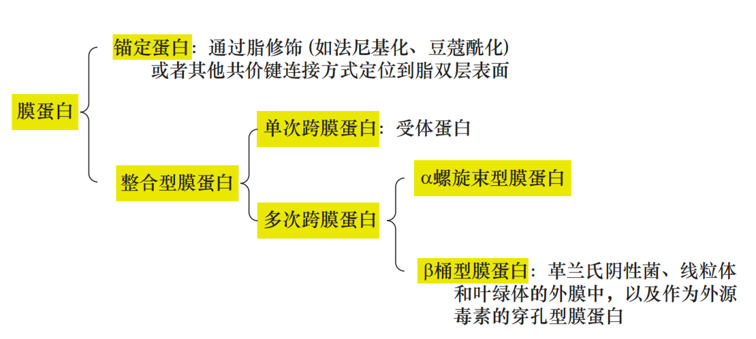
圖2:膜蛋白分類
此外,具有天然構象的全長膜蛋白因其結構的特殊性和功能的不可替代性,使其成為連接細胞內外信號與生命活動的核心樞紐,為揭示 “跨膜區 - 胞內區 - 胞外區” 的相互調控機制提供關鍵依據,補了截斷體研究的局限性。
三、跨越屏障:膜蛋白研究的三大挑戰
由于膜蛋白的高度疏水性使其容易在水環境中聚集,因此研究膜蛋白通常具有挑戰性,尤其是全長膜蛋白,獲取其完整結構,一直是結構生物學領域的巨大挑戰。
1.表達困難:當利用傳統的細胞系統(如細菌、昆蟲或哺乳動物細胞)來表達膜蛋白時,其疏水的跨膜區很容易被識別為“錯誤折疊”,導致蛋白聚集、形成包涵體,甚至對宿主細胞產生毒性,最終無法獲得大量、正確折疊的蛋白。
2.提取與純化困難:為了將膜蛋白“提取”出來進行研究,必須使用去垢劑來模擬其原生膜環境。這個過程非常苛刻,很容易破壞蛋白的天然結構,使其失去活性。提取出來的蛋白也不穩定,容易變性或聚集。
3.結構解析困難:經典的X射線晶體學需要獲得高質量的三維晶體。但對于構象動態變化的全長膜蛋白來說,使其形成有序的晶體陣列極為困難。
這導致開發周期長、表達效率不穩定、普適性差。對于需要快速驗證的大量候選蛋白,傳統的細胞工廠無法進行與之匹配的高通量并行制造。因此,亟需一種新的蛋白合成方式來擺脫活細胞的局限性。
四、破局之道:無細胞表達系統如何“另辟蹊徑”
無細胞蛋白質合成(CFPS)系統跳出了活細胞的限制,直接在體外利用細胞提取物合成目標蛋白,如同將細胞內的生命合成“生產線”搬到了“試管”中。合成體系開放,研究人員可自由調整離子強度、輔因子濃度;合成過程快速高效,且天然適配高通量操作,可在微孔板中并行合成與測試數十至上百個候選序列。此外,無細胞體系無生存壓力,可通過外源添加去垢劑或納米盤等成分,為膜蛋白提供類似天然膜環境的條件,有效維持其結構和功能。
【技術實踐】:珀羅汀生物依托自主知識產權的無細胞蛋白表達技術,膜蛋白表達成功率接近100%。通過在表達的體系中加入去垢劑或納米盤的方式保持膜蛋白的穩定性,使得膜蛋白更易表達純化。我們成功表達過的膜蛋白包括細胞色素酶、呼吸鏈酶、ligand receptor等。
無細胞+去垢劑平臺
通過在無細胞體系中直接添加去垢劑,可以為膜蛋白跨膜區提供疏水環境,輔助膜蛋白形成正確構象,實現全長跨膜蛋白可溶表達。
跨膜蛋白表達
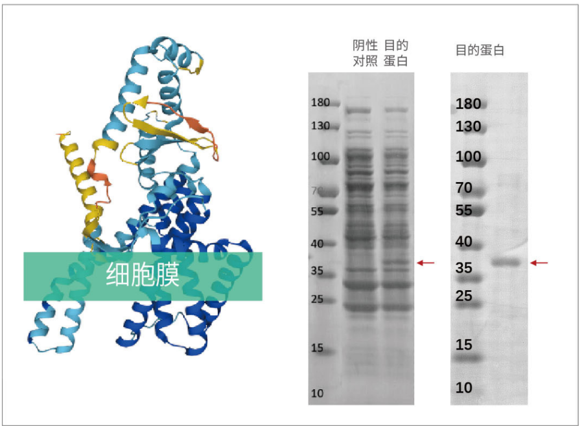
圖3:七次跨膜蛋白

圖4:四次跨膜蛋白
無細胞+納米盤平臺
通過在無細胞體系中加入膜支架蛋白與磷脂,形成類似細胞膜的納米盤結構,可以使合成的膜蛋白直接組裝進納米盤,高疏水性的跨膜區穩定插入脂雙層,獲得高穩定性、高活性、接近天然構象的全長膜蛋白。
跨膜蛋白表達
跨膜蛋白表達
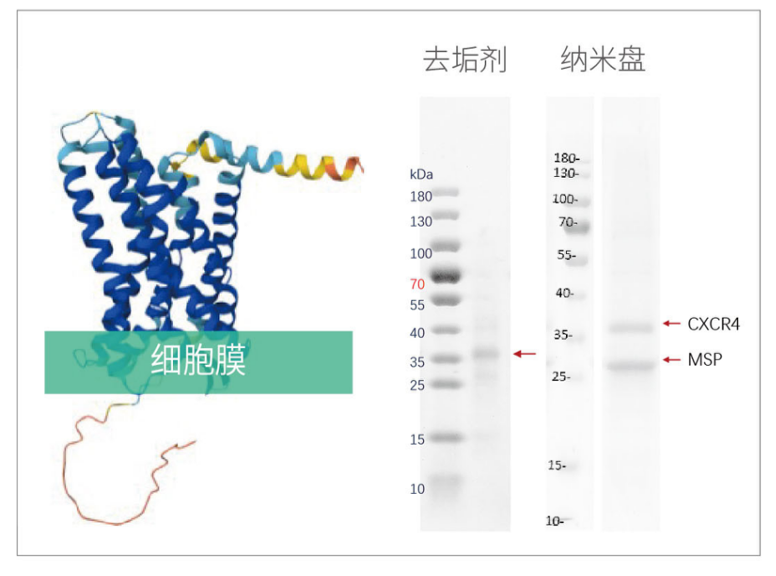
圖5:七次跨膜蛋白
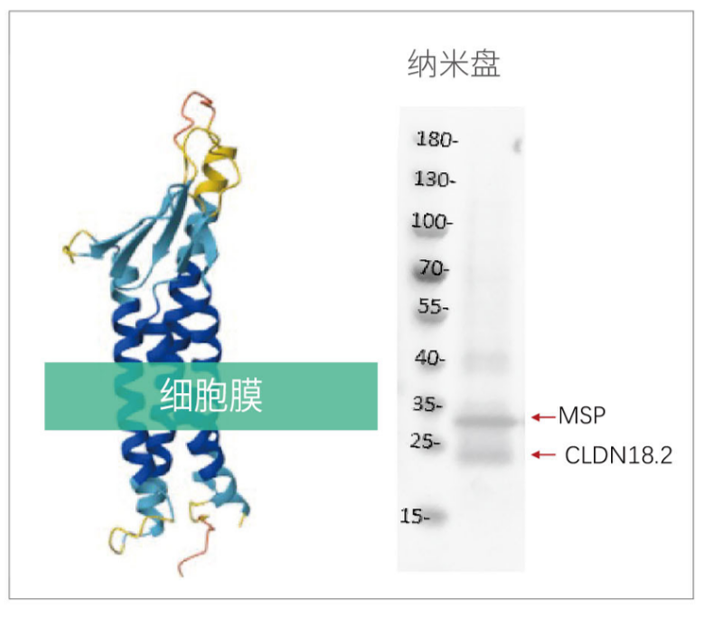
圖6:四次跨膜蛋白
五、技術前景與展望
隨著無細胞蛋白表達技術的成熟,其市場規模也在穩步增長。QYResearch調研顯示,2023年全球無細胞蛋白表達市場銷售額達到了15億元,預計2030年將達到23億元。這一增長背后是制藥、生物技術領域對快速蛋白質開發工具的迫切需求。
人工智能與無細胞蛋白合成的結合,正在進一步加速這一領域的發展。AI已在蛋白質結構預測、序列生成與功能設計方面展現出強大威力,而無細胞體系則有潛力成為連接數字世界與物理實體的高效橋梁,將AI的海量設計方案快速轉化為可測試的真實分子。將人工智能的設計能力與無細胞體系的快速合成能力相結合,被視為突破蛋白質工程瓶頸的關鍵。
作為一項技術,無細胞蛋白表達系統正在重塑膜蛋白研究的格局。從VLP平臺、Nanodisc技術到我司的無細胞蛋白表達系統,這些創新工具使科學家能夠在更貼近天然環境的條件下研究膜蛋白的結構與功能。隨著人工智能與無細胞系統的深度融合,以及新方法的不斷涌現,我們將有望揭開更多膜蛋白的神秘面紗,加速從基礎研究到藥物開發的轉化進程,最終為人類疾病治療帶來新的突破。
參考資料:
1.膜蛋白結構動力學(第二版);
2.Zhu, Jingyi, and Peilong Lu. “Computational design of transmembrane proteins.” Current opinion in structural biology vol. 74 (2022): 102381. doi:10.1016/j.sbi.2022.102381;
3.2024-2030年全球及中國無細胞蛋白表達行業運營動態及發展潛力研究報告。
微信掃一掃
